Validación de los analizadores de carbono orgánico total en línea para pruebas de liberación utilizando ICH Q2
Introducción
A medida que la industria farmacéutica busca reducir el número de pruebas de laboratorio de control de calidad y los costes asociados, la fiabilidad de los resultados de los analizadores de COT en línea para la liberación de productos vuelven a estos instrumentos cada vez más atractivos. La Conferencia Internacional sobre Armonización (ICH) es un grupo de trabajo de expertos con representación de las farmacopeas de Estados Unidos2, Europa3 y Japón4. En su guía armonizada tripartita ICH Q21, Validación de Procedimientos Analíticos, realizan un resumen de las características a tener en consideración durante la validación de procedimientos analíticos incluidos como parte de las aplicaciones de registro enviadas dentro de la UE, Japón y EE. UU. Este documento examina cómo podrían aplicarse estas características en los analizadores de carbono orgánico total (COT) en línea, a fin de que se puedan utilizar para proporcionar datos de pruebas de liberación de agua para inyección (API) y agua purificada (AP).
Para ver el seminario web sobre este tema, desplácese hasta el final de esta página.
Descripción general de los analizadores de COT
Los analizadores de COT miden uno de los cuatro atributos clave de calidad exigidos por las farmacopeas. El análisis de COT es una prueba no específica, es decir, es simplemente una medición del carbono que se encuentra en cualquier compuesto orgánico en agua, no le puede decir qué tipo de molécula orgánica está presente. Un analizador de COT de calidad farmacéutica utiliza luz ultravioleta (UV) para oxidar las moléculas orgánicas a fin de liberar los átomos de carbono presentes y luego mide la diferencia de conductividad del agua debida al dióxido de carbono resultante.
El COT debe calcularse midiendo el carbono inorgánico total (CIT) y el carbono total (CT) y restando uno del otro.
CT - CIT = COT
Figura 1. El CIT y el CT se miden y el COT se calcula
El capítulo EP 2.2.44 de la Farmacopea Europea sobre el COT para AP (agua farmacéutica) y API (agua para inyección) demanda la oxidación completa de la molécula orgánica para obtener un análisis preciso del COT, es decir, si algunos de los átomos de carbono no se oxidasen y permanecieran unidos a la molécula orgánica, estos no se medirían y el analizador de COT informaría menos COT de lo debido. Por este motivo, es importante que el analizador de COT sea capaz de detectar cuándo se ha completado la oxidación antes de informar de los niveles de COT.
Los resultados de COT se notifican en partes por billón (ppb), que en este caso es la masa (peso) de carbono orgánico por litro de agua. Las moléculas orgánicas complejas de cadena más larga contendrán más átomos de carbono que las moléculas orgánicas de cadena corta, por lo que el analizador de COT notificará los números equivalentes de las moléculas de cadena larga y cadena corta de manera diferente, con el COT notificado de los compuestos orgánicos de cadena larga proporcionando resultados de COT más altos.
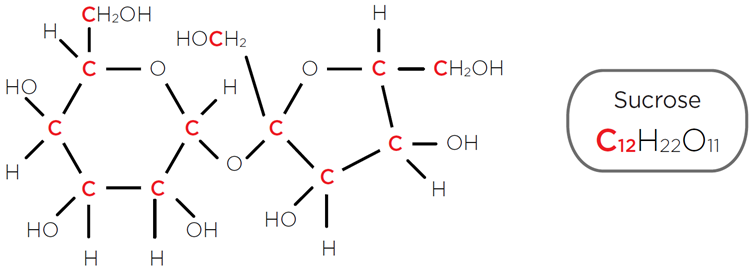
Figura 2.La molécula orgánica de la sacarosa contiene 12 átomos de carbono
Descripción de la ICH Q2
La directriz ICH Q2 cubre tres aplicaciones diferentes de los analizadores: Identificación, pruebas de impurezas y pruebas de ensayo. Los analizadores de COT que se utilizan para probar la contaminación del AP y API caen naturalmente bajo la clasificación de aplicación para pruebas de impurezas. La ICH Q2 continúa con la diferenciación entre las características de validación requeridas para los analizadores utilizados para pruebas de límite de impurezas y aquellos utilizados para análisis cuantitativo de impurezas. Características de validación de la ICH Q2 que deben tenerse en cuenta:
- Exactitud
- Precisión
- Repetibilidad
- Precisión intermedia
- Especificidad
- Límite de detección
- Límite de cuantificación
- Linealidad
- Intervalo
Los analizadores de COT en línea tienen el propósito de determinar que no se supere el límite compendial de 500 ppb, pero también se utilizan para determinar las tendencias en los niveles de COT y, como tales, entran en el ámbito de las características de validación aplicadas tanto a los analizadores de pruebas cuantitativas como a los de pruebas de límite.
La lista de viñetas anterior enumera las características de validación que se utilizan para determinar la idoneidad de un analizador de COT. Aunque la robustez no figura en la lista, la ICH Q2 recomienda este aspecto de la validación durante la cualificación inicial del analizador y en los períodos adecuados a partir de entonces.
Demostración de cumplimiento de la ICH Q2
Exactitud
La ICH Q2 sugiere que la exactitud se puede establecer determinando la cercanía del acuerdo entre el analizador y un valor de referencia aceptado. Para los analizadores de COT, esto se puede lograr realizando una validación de calibración, p. ej., ejecutando estándares de COT certificados como muestras al azar y determinando si los resultados proporcionados por el analizador se encuentran dentro de límites de rendimiento aceptados/especificados. Naturalmente, el analizador debería haber pasado por un ajuste de calibración antes de realizar esta prueba, es decir, debería haberse realizado el procedimiento normal de ajuste de calibración recomendado por el fabricante.

Figura 3. Determinación de la exactitud del analizador de COT utilizando estándares de COT certificados
La ICH Q2 sugiere que la exactitud se debería demostrar utilizando 3 réplicas de 3 concentraciones, como se muestra en la Figura 3.
Precisión
La validación de los analizadores para la cuantificación de impurezas incluye una investigación de precisión. La ICH Q2 recomienda que la determinación de precisión de la repetibilidad se valide utilizando 3 réplicas de cada uno de los 3 estándares certificados a diferentes concentraciones. También recomienda que se valide el efecto de los cambios ambientales y de error humano en la precisión intermedia del analizador.
Especificidad
Esto establece la capacidad del analizador de medir el analito de interés en presencia de sustancias potencialmente interferentes. En el caso de un sistema de AP o API moderno, el desafío que enfrentan los analizadores de COT es que los niveles de COT son relativamente pequeños, a menudo por debajo de 30 ppb, mientras que los niveles de CIT y CT son comparativamente altos, a veces entre 1000 ppb y 2000 ppb. Como se indica en la Figura 1, los analizadores de COT miden el CIT y CT para luego calcular el COT. Los pequeños errores de medición de CT y CIT pueden provocar errores importantes en el valor de COT calculado. Este problema es más evidente en los analizadores de COT que tienen sensores independientes para medir CT y CIT; consulte el ejemplo en la Figura 3.
| Ejemplo: | Results (Resultados): | ||
| CT real | 1000 ppb | CT medido | 980 a 1020 ppb |
| CT real | 990 ppb | CIT medido | 970 a 1010 ppb |
| COT real | 10 ppb | COT calculado | -30 a 50 ppb |
| Error de medición del sensor +/-2 % | |||
Figura 4. Error en en COT notificado debido a interferencia del CIT
Límite de detección
Las farmacopeas establecen que los analizadores de COT adecuados deben tener un límite de detección (LOD) de ≤50 ppb. Validar un nivel tan bajo de COT es difícil utilizando los estándares de COT rastreables, ya que por lo general estos no están disponibles. De igual manera, no es práctico que intente hacer su propia solución de COT a 50 ppb. La ICH Q2 sugiere que una alternativa es calcular el LOD ejecutando múltiples muestras de una solución de COT en blanco (<100 ppb de="" cot="" según="" las="" farmacopeas)="" y="" utilizando="" la="" desviación="" estándar="" entre="" las="" mediciones="" para="" calcular="" el="" lod;="" consulte="" la="" figura="">
LOD = 3,3 σ / S
donde LOD = límite de detección
σ = La desviación estándar de los resultados de la muestra en blanco
S = La pendiente de la curva de calibración
Figura 5. Cálculo del límite de detección
Límite de cuantificación
Este es el nivel más bajo de COT que el analizador puede medir con exactitud y al que puede notificar valores de COT. Al igual que el LOD, esto puede resultar difícil de establecer utilizando estándares de COT rastreables, ya que por lo general no están disponibles. La ICH Q2 nuevamente sugiere que un método aceptable para validar esta característica es ejecutar múltiples análisis de muestras en blanco y utilizar la desviación estándar para calcular el límite de cuantificación; consulte la Figura 6.
QL = 10 σ / S
donde QL = límite de cuantificación
σ = La desviación estándar de los resultados de la muestra en blanco
S = La pendiente de la curva de calibración
Figura 6. Cálculo del límite de cuantificación
Como se puede observar a partir de las fórmulas de las Figuras 5 y 6, el límite de cuantificación es aproximadamente tres veces el límite de detección.
Linealidad
La linealidad, aplicada a los analizadores de COT, es la capacidad de dibujar una línea recta a través de tres o más puntos en la curva de calibración del analizador de COT. Esta se puede determinar ejecutando tres o más estándares de COT certificados en el analizador. Mientras el coeficiente de correlación de linealidad sea >0,99, se puede decir que el analizador tiene una respuesta lineal. El coeficiente de correlación se puede calcular durante la calibración si se utilizan tres o más estándares de calibración.
Intervalo
Los analizadores de COT de grado farmacéutico están diseñados para demostrar que el límite de 500 ppb definido en la farmacopea no se ha superado. El intervalo aceptable de un analizador de COT farmacéutico se establece confirmando que el procedimiento analítico proporcione un grado aceptable de linealidad, exactitud y precisión al aplicarse a muestras conteniendo cantidades de COT dentro, o en los valores extremo, del intervalo especificado del procedimiento analítico. Dado que el máximo especificado es de 500 ppb, la linealidad, la precisión y la exactitud deben demostrarse alrededor de este máximo. La ICH Q2 recomienda realizar pruebas con estándares de COT certificados de al menos +/-20 % del máximo. Es una práctica habitual utilizar estándares de calibración de 250, 500 y 750 ppb para determinar la linealidad y exactitud del analizador de COT en torno al intervalo máximo de 500 ppb, ya que éste excede el +/-20 % requerido, dando un +/-50 % del máximo.
Robustez
La característica de robustez se utiliza para demostrar la fiabilidad de un analizador con respecto a variaciones deliberadas en los parámetros del método. En el caso de los analizadores de COT, las farmacopeas de Estados Unidos y Europa sugieren que esto se establezca mediante la prueba de idoneidad del sistema (SST), en la que se prueba la respuesta del analizador a los estándares de COT en materiales orgánicos deliberadamente diversos para garantizar que no haya una gran variación en los resultados. Las soluciones de sacarosa de fácil oxidación y benzoquinona difícil de oxidar, contienendo ambas 500 ppb de carbono, se analizan en el analizador de COT. Para demostrar que el analizador es robusto, los resultados notificados de ambas soluciones SST deben estar a +/-15 % entre sí.
Cómo demuestra el analizador de COT en línea PAT700 de Beckman Coulter el cumplimiento de la ICH Q2
El PAT700 de Beckman Coulter está diseñado para apoyar el cumplimiento de la ICH Q2 al utilizar lo siguiente:
| Características ICH Q2 | Cómo demuestra el PAT700 el cumplimiento de la ICH Q2 |
| Exactitud | Validación de calibración utilizando tres réplicas de tres estándares de COT certificados |
| Precisión | |
| Repetibilidad | Validación de calibración utilizando tres réplicas de tres estándares de COT certificados |
| Precisión intermedia | Los PNT automatizados y preprogramados combinados sin introducción manual de datos y cálculos de aceptación/fallo eliminan las oportunidades de error humano |
| Especificidad | Poseer un sensor de medición único para CIT y CT significa que el PAT700 no se ve afectado por la presencia de grandes cantidades de CIT, a diferencia de los analizadores de COT que utilizan sensores independientes para medir CIT y CT y luego calcular el COT |
| Límite de detección | Procesa múltiples muestras en blanco y calcula utilizando la fórmula de ICH Q2 |
| Límite de cuantificación | Procesa múltiples muestras en blanco y calcula utilizando la fórmula de ICH Q2 |
| Linealidad | Utilice el PNT de calibración integrado, que calcula y notifica automáticamente el coeficiente de correlación de linealidad y solo permite un “aprobado” si este es >0,990 |
| Intervalo | Estándares de calibración de 250, 500 y 750 ppb para determinar la linealidad y la exactitud del analizador de COT alrededor del límite de prueba de 500 ppb |
| Robustez | Utilice la prueba de idoneidad del sistema para demostrar que el analizador es fiable y no es susceptible a errores al realizar variaciones deliberadas en los parámetros del método |
Referencias
- International Conference on Harmonisation of Technical Requirements for Registration of Pharmaceuticals for Human Use VALIDATION OF ANALYTICAL PROCEDURES: TEXT AND METHODOLOGY ICH Q2 9, ICH Secretariat, Chemin des Mines, 1202 Geneva, Switzerland http://www.ich.org/products/guidelines/quality/article/quality-guidelines.html
- U.S. Department of Health and Human Services Food and Drug Administration United States Pharmacopoeia U.S. Department of Health and Human Services Food and Drug Administration Center for Drug Evaluation and Research (CDER) Center for Biologics Evaluation and Research (CBER) Office of Regulatory affairs (ORA) Division of Drug Information, HFD-240 Center for Drug Evaluation and Research Food and Drug Administration 5600 Fishers Lane, Rockville, MD 20857 USA
- Council of Europe European Directorate for the Quality of Medicines & Healthcare European Pharmacopoeia (Ph. Eur) 9th Edition. EDQM Council of Europe, 7 allée Kastner, CS 30026, F-67081 Strasbourg, France https://www.edqm.eu/en/european-pharmacopoeia-9th-edition
- The Japanese Ministry of Health Labour and Welfare, The Japanese Pharmacopoeia, Seventeenth Edition, Pharmaceuticals and Medical Devices Agency, Shin-Kasumigaseki Building, 3-3-2 Kasumigaseki, Chiyoda-ku, Tokyo 100-0013 Japan https://www.pmda.go.jp/english/rs-sb-std/standards-development/jp/0019.html

