Mediciones automatizadas de concentración y viabilidad de las células sanguíneas del cordón umbilical utilizando el VI-CELL XR
Introducción

Las células madre, debido a su diferenciación en células sanguíneas maduras, son la clave del éxito de los trasplantes de médula ósea. Recientemente, se ha descubierto que la sangre del cordón umbilical es también una fuente abundante y rica de células madre hematopoyéticas.(1). Por lo tanto, se utiliza tanto la sangre de la médula ósea como la del cordón umbilical en el tratamiento de numerosos cánceres, trastornos inmunológicos y ciertas enfermedades genéticas.
Sin embargo, las células madre de la sangre del cordón umbilical ofrecen importantes ventajas importantes con respecto a las células aisladas de la médula ósea. Las células madre de la sangre del cordón umbilical son mucho más fáciles de asegurar, dado que se obtienen de inmediato del cordón umbilical y la placenta en el momento del parto, mientras que obtener células madre de la médula ósea requiere un procedimiento quirúrgico (normalmente bajo anestesia general). Para que un trasplante de médula ósea tenga éxito, debe haber una coincidencia casi perfecta de proteínas tisulares, denominadas antígenos, entre el donante y el receptor. Las células madre de la sangre del cordón umbilical se “asimilan” incluso cuando hay coincidencias parciales.(2) Por lo tanto, más receptores se benefician de las células madre infundidas de la sangre del cordón umbilical.
En la actualidad, muchas instalaciones ofrecen a los padres la opción de almacenar, o preservar en banco de células, la sangre del cordón umbilical del recién nacido.(3) Cuando las células se depositan (normalmente en nitrógeno líquido), se deben analizar dos parámetros de manera precisa. Estas mediciones son la concentración celular y el porcentaje de viabilidad celular.(4). Estas mediciones se realizan antes de su almacenamiento y después del proceso de descongelación. Las células pueden disminuir tanto en número como en viabilidad, principalmente debido al crioconservante empleado en el proceso de congelación (normalmente DMSO).
El VI-CELL XR (Figura 1) automatiza el método manual de exclusión de colorante vital azul tripán que se utiliza para determinar la viabilidad celular. Además, el instrumento proporciona una medición objetiva de la concentración celular. Como se mencionó, estos son los dos parámetros críticos que se requieren en el proceso de preservación de células sanguíneas del cordón umbilical. El objetivo de este trabajo fue describir un método para la preparación de muestras de sangre del cordón umbilical y el desarrollo de un tipo de célula, y un conjunto preciso de parámetros para el instrumento, en este caso el Vi-CELL XR.
Materiales y métodos
El laboratorio SAS de Beckman Coulter obtuvo una muestra de sangre de cordón umbilical del Baptist Hospital, Miami, FL. La sangre se diluyó 1:1 utilizando solución salina tamponada con fosfato a temperatura ambiente. Para aislar las células mononucleares se utilizó el método estándar de separación de gradiente Ficoll*.(5). Las células aisladas se lavaron una vez en PBS y se resuspendieron en 2 ml de Isoflow* (Isoton* II). Se preparó una dilución 1:10 de la suspensión celular colocando 100 µl de células en 900 µl de Isoflow en un pocillo de muestras Vi-CELL™ estándar. El Vi-CELL XR se utilizó para desarrollar el tipo de célula sanguínea del cordón umbilical. Antes de analizar la muestra, se realizó un ensayo del control de concentración de Vi-CELL™.Resultados
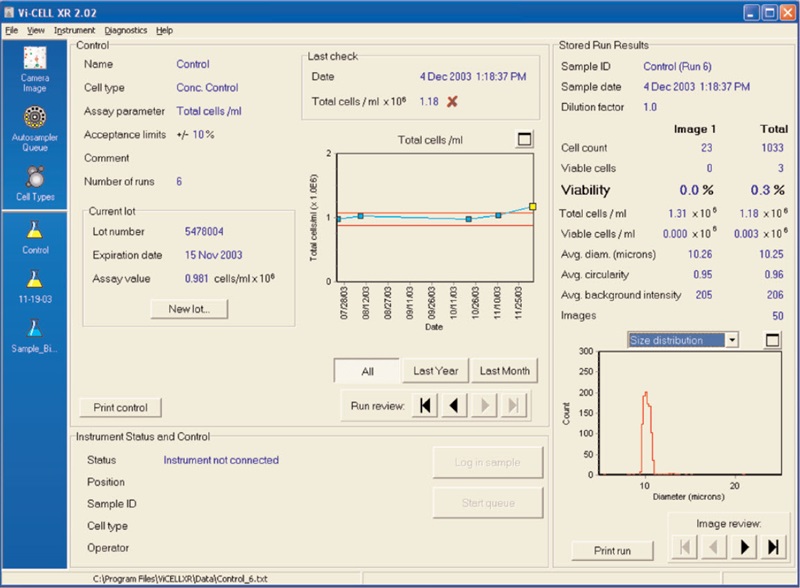
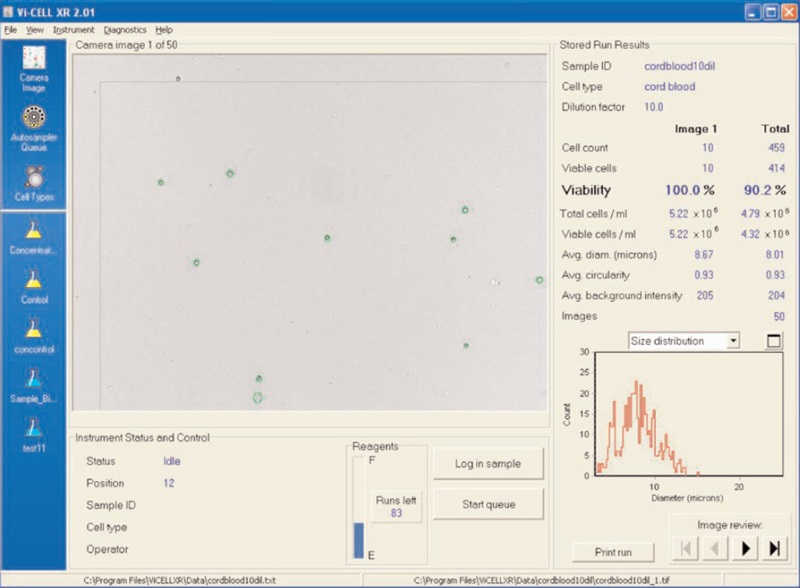
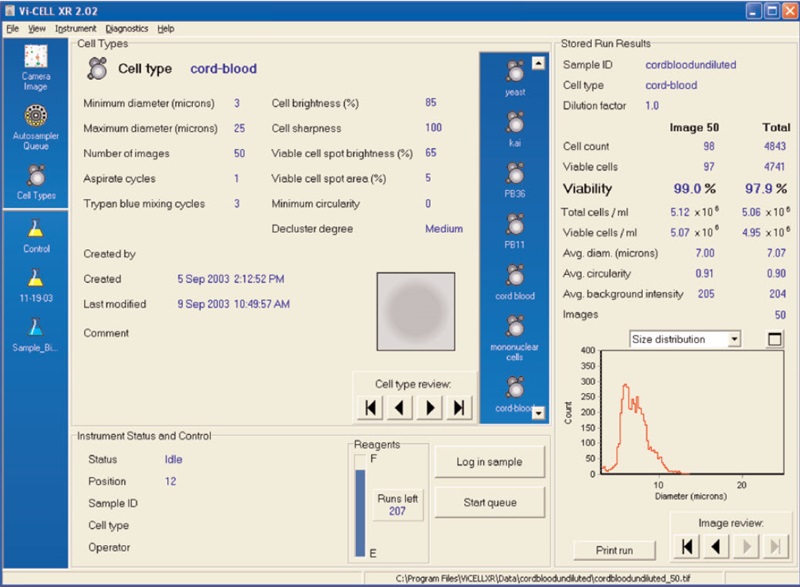
La Figura 2 muestra los resultados del control de concentración de Vi-CELL. La Figura 3 ilustra una imagen de células sanguíneas del cordón umbilical en el Vi-CELL XR. La Figura 4 muestra los parámetros de tipo de célula que se utilizaron para analizar las células sanguíneas del cordón umbilical. El intervalo de tamaños se estableció de 3 a 25 micras. Brillo de la célula: 85; nitidez celular: 100; brillo del punto de célula viable: 65; área del punto de célula viable: 5.Conclusiones
Las infusiones de células madre de la sangre del cordón umbilical tienen ventajas significativas en los trasplantes de médula ósea. La viabilidad y la concentración de las células sanguíneas del cordón umbilical se pueden analizar utilizando el Vi-CELL XR. Se determinaron los ajustes de tipo de célula para las muestras de sangre del cordón umbilical. Intervalo de tamaños de 3 a 25 micras. Parámetros de obtención de imágenes: Brillo de la célula: 85; nitidez celular: 100; brillo del punto de célula viable: 65; área del punto de célula viable: 5.
Referencias
- Kurtzberg, J., Laughlin, M., Graham, M. L., et al. Placental blood as a source of hematopoietic stem cells for transplantation. Blood 90, 4665-4678 (1997).
- Zeigner, U., et al. Unrelated umbilical cord stem transplantation for x-linked immunodeficiencies. Journal of Pediatrics 134, No. 4, 570-573 (2001).
- American Academy of Pediatrics Work Group on Cord Blood Banking. Cord blood banking for potential future transplantation: subject review. Pediatrics, Vol. 104, No. 11, 116- 118 (1999).
- Fiorino, Susan, Johns Hopkins University, The Sidney Kimmel Comprehensive Cancer Center. Personal Communication.
- Boyum, A. Separation of white blood cells, Nature 204, 793-794 (1964).

